Las características de los ácidos y las bases se resumen en el siguiente cuadro:
| Ácidos | Bases | |
| ▪Tienen sabor agrio (ácido). | ▪Tienen sabor amargo. | |
| ▪Reaccionan con ciertos metales, como Zn, Mg o Fe, para dar hidrógeno | ▪Reaccionan con las grasas para dar jabones. | |
| ▪Reaccionan con las bases para dar sales | ▪Reaccionan con los ácidos para dar sales. | |
| Son sustancias ácidas: el ácido clorhídrico (HCl); el ácido bromhídrico (HBr); el ácido nítrico (HNO3); el ácido carbónico (H2CO3) y el ácido sulfúrico (H2SO4), entre otros | Son sustancias básicas el hidróxido de amonio o amoniaco disuelto en agua (NH4OH); y los hidróxidos de los metales alcalinos (LiOH, NaOH, KOH,...) y alcalinotérreos, como el Ca(OH)2, y Mg(OH)2, entre otros |
Para distinguir si una sustancia es ácida o básica, se utiliza la escala de pH, comprendida entre el 1 y el 14:
- Si una sustancia tiene un pH igual a 7, se dice que es neutra, ni ácida ni básica (por ejemplo, el agua pura).
- Si una sustancia tiene un pH menor que 7, tiene carácter ácido.
- Si una sustanica tien un pH mayor que 7, tiene carácter básico.
En los laboratorios y aquellos otros lugares donde es necesario determinan esta propiedad (como en un análisis de agua potable, por ejemplo), se utiliza un indicador ácido-base, que es una sustancia que presenta un color distinto según sea el pH del medio. Algunos ejemplos se muestran en las dos tablas siguientes:
| Indicadores | Color en medio ácido | Color en medio básico | 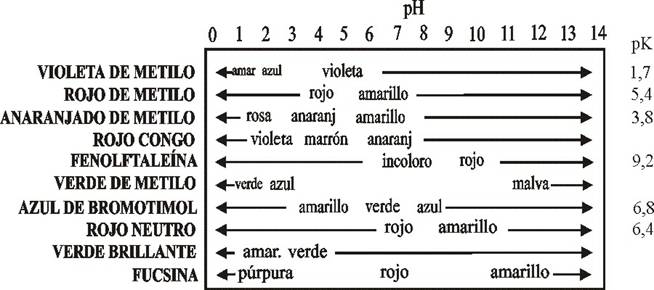 |
| Naranja de metilo | Naranja | Amarillo | |
| Fenolftaleina | Incoloro | Rosa | |
| Azul de bromotimol | Amarillo | Azul | |
| Tornasol | Rojo | Azul |
Para ahorrar tiempo y trabajo, se utiliza mucho el papel indicador universal, que es un papel impregnado con una mezcla de indicadores y que adquiere un color distinto según los distintos pH.
6.2- Neutralización
Cuando entran en reacción un ácido (por ejemplo, HCl) y una base (NaOH), el primero se disocia liberando H+ y Cl-, mientras que el segundo se disocia en Na+ y OH-. Los iones Cl- y Na+ se unen formando una nueva sustancia neutra (en este caso NaCl), llamada sal y los iones H+ y OH- se unen por su parte para forman H2O, es decir, agua.
| acido + base → sal + agua |




